白血病
白血病俗稱血癌,是所有血液疾病中最令大家所熟悉和害怕的。為了幫助罹患白血病的病人和家屬可以以正確的觀念與方式來面對和認識疾病,我們會在下面的文章中加以介紹,期望能對病人及家屬有所助益。
血球簡介 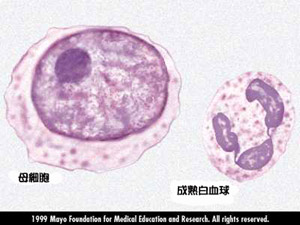
血液大約佔人體體重的 7~10%,在成人約有五公升的血液。血液主要由兩種成份所組成: 55%的血漿和45%的血球。血球又分為:紅血球白血球血小板。其中白血球依其形狀和功能再細分為嗜中性白血球、嗜酸性白血球、嗜鹼性白血球淋巴球和單核球。 血液對人體的重要功能 : 1.運送氧氣 紅血球負責將氧氣運送至全身細胞,供進行氧化作用產生能源,細胞代謝產生二氧化碳則藉由血漿排出體外。 2.運送養份和荷爾蒙 可將消化道收的養份或肝臟合成的養份及內分泌系統所分泌的荷爾蒙,運送到各特定的器官以發揮作用。 3.消滅病原體
白血球及抗體可將侵犯人體之病原體消滅。 4.止血 血小板及凝血因子可在血管受到傷害破裂時,促使出血處發生凝血作用,防止繼續出血。 5.維持體內酸鹼平衡 血液可循環全身,幫助維持體內的環境在達到平衡的狀態之中。 人體的造血過程,即是血球的生成過程,人體內的所有血球都是由骨髓內的幹細胞開始製造,幹細胞在體髓內經過連續的分裂和成熟分化過程,最後形成成熟的血球,再釋放到週邊的血流中,於全身循環。 何謂白血病 白血病是指人體的主要造血系統 -骨髓產生了癌化病變。其白血球失去了正常血球細胞應有的分化能力及老化死亡現象,所以造成這些不正常的白血球不斷的增生,逐漸的取代了骨髓內的正常造血細胞,於是將整個骨髓佔據並偏佈於血液中。當癌細胞佔據骨髓後,它所影響的已經不是只有白血球而已,紅血球血小板的功能同時也會受影響。 白血病之種類 白血病依照臨床病程進展的速度和癌細胞的成熟度可分為:急性白血病及慢性白血病,再依細胞的來源及型態特徵,細分為急性骨髓性白血病、慢性骨髓性白血病、急性淋巴球性白血病和慢性淋巴球性白血病。 1.急性骨髓性白血病(AML) 急性骨髓性白血病好發於成年人,約有 75~80%的病人超過20歲。依英美法合作小組(French American British cooperative group ; FAB Classification)的分類,將急性骨髓性白血病細分為M1~M7型。M1型是急性未成熟骨髓芽球性白血病;M2是急性成熟骨髓芽球性白血病;M3急性多顆粒前骨髓細胞性白血病;M4急性骨髓單核球性白血病;M5是急性單核球性白血病;M6是急性紅血球性白血病;M7是急性巨核細胞性白血病。 2.慢性骨髓性白血病(CML)
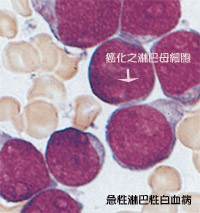
慢性骨髓性白血病是源於造血母細胞的一種惡性腫瘤。費城染色體 (Ph chromosome) 指的是一個變短的第22對染色體,它出現在90-95%的 慢性骨髓性白血病病例中,可說是慢性骨髓性白血病的疾病指標。 3.急性淋巴球性白血病(ALL) 急性淋巴球性白血病好發於 10歲以下兒童,成年人約佔20%左右。依FAB分類,又可將其分為L1、L2、L3型。 4.慢性淋巴球性白血病(CLL) 慢性淋巴球性白血病好發 50歲以上中老年人。淋巴球可分為B細胞及T細胞,所以慢性淋巴球性白血病也可分為這兩型之其中一型。 白血病之致病因素 1.放射線 正常人罹患白血病的機率在兩萬五千分之一左右,但曾身處在原子彈爆炸圈一公里以內的居民,倘若倖存,其於數年之後罹患白血病的機率就高達六十分之一左右。另外懷孕婦女接受腹部 X照射,新生兒罹病率也較高。 2.化學藥劑 長期接觸有機苯 (Benzene)的工人,或曾接受過含氫化合物(Alkylating agents)化學治療的病人,其罹患白血病的機率也比正常人高。 3.遺傳或基因突變 先天染色體異常,如唐氏症 (Down's syndrome)布倫氏症候群(Bloom's syndrome)等先天疾病可能會誘導白血病的發生。如家中有人曾罹病其機率較高。 4.自體免疫性疾病 自體免疫的缺陷可能與慢性淋巴球性白血病有關。 5.病毒咸染 目前已知第一型人類 T淋巴球細胞性病毒HTLV-I病毒感染與成年型T細胞白血病有關。 白血病之症狀 1.急性白血病 一般來勢兇兇,常見的臨床表現有不明原因的持續性發燒 :不成熟的白血球快速生成,新陳代謝加速之故。容易出血:包括流鼻血牙齦出血皮膚出現點狀或塊狀出血女性會出經血過多或是不止的情形。貧血:容易疲倦臉色蒼白因紅血球減少,血紅素降低所致。關節疼痛:常發生於膝蓋部位。其它如牙齦腫脹、體重減輕、腹部飽脹感等不適情形也很常見。 2.慢性骨髓性白血病 依其病程可分為慢性期、加速期及芽球期。慢性期常見的症狀為疲倦、發燒、體重減輕、貧血等,不正常的出血較少見,但約有 20%的病患不會出現任何症狀。當疾病在加速期,會出現肝脾腫大、不正常白血球或血小板增生。芽球期病況其類似急性白血病。 3.慢性淋巴球性白血病 疾病初期病患幾乎無任何症狀,但免疫功能明顯減退,部病患會出現帶狀泡疹。另外隨著病程進展,病患同樣會出現淋巴結與肝脾腫大,部份患者可能會因腹膜腔後淋巴結腫大而引起腸胃道與泌尿道阻塞的情形。甚至有些病患會出現自體免疫溶血性貧血及血小板缺乏症。 白血病之診斷 1. 血液常規檢查 白血球數目增高,可能增加到數十萬以上,且出現大量不成熟之白血球。紅血球及血小板的數目可能會下降,血紅素也偏低。 2. 周邊血液抹片 抹片結果呈現出許多髓芽細胞,這些細胞就不熟成的白血球。 3. 骨髓穿刺切片檢查 骨髓穿刺的部位通常在胸骨或是骨盆腔處的腸骨脊來抽取,醫師會消毒皮膚後,注射局部麻醉劑,再以穿刺針穿過皮膚,並以特殊針頭鑽過骨頭,到達骨髓腔抽取少量骨髓血。 白血病之治療與副作用 化學治療 全身性化學治療為白血病最主要的治療方式,其它的治療包括放射線治療、骨髓移植及支持性療法等,以下依不同的白血病分類來說明其治療方式: 急性骨髓性白血病 近年來急性骨髓性白血病(Acute myelocytic leukemid, AML)化學治療及幹細胞移植之進步,約有20~60%已經可以治癒。目前積極尋求治療技術及觀念的改進,希望能更加提高治癒率。除了高劑量的化學治療外,在緩解期間是否需要鞏固療法及維持療法以達到total cell kill的觀念,以及最近急性前骨髓性白血病的分化誘導療法,不用高劑量的化學治療而只以全反式維甲酸的誘導分化療法,也能得到極高的緩解率等等,使我們反省到急性骨髓性白血病的治療是不是一定需要強力以及長期持續性的化學治療。 -7+3療法
此化學療法為急性骨髓性白血病的標準療法,使用Cytarabine (Ara-C, 100~200mg/m2/day, iv連續注射7日),合併daunorubicin (DNR, 45mg/m2/day, iv連續注射3日),結果得到60%到80%的完全緩解率,然而病人仍須接受鞏固療法或長期性的維持療法。其長期存活率約為20~30%。
- 5+2療法
以idarubicin( 5~10mg/m2/day, iv連續注射2日)取代DNR的方式,骨髓抑制較嚴重但效果較佳。 - 高劑量療法(high-dose Ara-C treatment )
以高劑量Cytarabine作為鞏固療法比傳統的療法可以改善病患之預後。但是使用高劑量Ara-C治療,其毒性明顯增加,老年患者可能因無法承受其毒性而致死亡。由於急性骨髓性白病患不一定能夠接受骨髓移植治療,因此對較為年輕且體能狀況)較佳的病患而言,採用高劑量Ara-C來作為急性骨髓性白血病之誘導緩解治療,可以明顯延長完全緩解期,並增加五年之無病復發率,似乎是一項不錯的選擇。但這種治療只對第十六對染色體異常、t(8:21)及雙套染色體(diploid)異常的病人有效,對t(15:17)異常者則較不適用。 - 分化誘導治療 急性前骨髓性白血病是急性骨髓性白血病中相當特別之一亞型,於傳統誘導緩解化學治療時,常不需經過骨髓內白血病細胞完全清除的階段,使可以達到完全緩解。其特徵是它有一個特定的細胞融合基因PML-RAR-α(PML為promyelocytic Leukemia gene, RAR-α是Retinoic acid receptor gene),是由帶有前骨髓性白血病基因的第十五對染色體和帶有維甲酸接受體α基因的第十七對染色體互相轉位而成,這個融合基因會製造促使骨髓母細胞在發展過程中的前骨髓期跳脫,以致無法成熟的一種蛋白質,而變成急性前骨髓性白血病。 在1988年,中國上海王博士利用全反式維甲酸(All-trans retinoic acid)來治療急性前骨髓性白血病,得到了高達90%的完全緩解,這個研究成果自然震驚了醫學界,也建立了第一個以分化誘導來治療癌症的案例,這就是所謂的「分化誘導療法」(differentiation therapy)° 。 骨髓母細胞有二種功能,一是「增殖」以維持族群(clone)的延續,二是「分化」成成熟細胞,以發揮其作用。這兩種功能必須維持平衡,假若增殖之功能下降,則細胞會朝分化成熟的方向走;相反的若分化成熟的功能被抑制住,則細胞會往增殖方向走。 白血病就是因為分化路徑被抑制而增殖,而它可能是因缺少某種物質之故,若能補充此物質如全反式維甲酸,則白血病之細胞便會往分化成熟之方向走去,而後死去,白血病便可因此而獲得解除。 這療法的缺點之一是一旦停止用藥,馬上會有復發的現象。所以法國臨床研究將此治療法加以改良,即最初診斷時以全反式維甲酸治療,以減少可能引發DIC(Disseminated intravascular coagulation)的機會。待病人緩解時再施以Ara-C +DNR化學療法,以避免可能的復發。而全反式維甲酸併用化學療法,其四年無病存活率高達76%,皆較單獨使用化學療法為優。 服用retinoic acid治療時,會引起所謂「retinoic acid syndrome」之副作用,需特別加以注意。此乃因白血病細胞分化成熟而導致白血球過多,而後壓迫到肺裏面去,使肺之血管阻塞,造成病患因氣喘或肺水腫而死。所以當服用retinoic acid時發現周邊血中白血球數急速增加時,應同時給予化學療法。 - 三氧化砷(arsenic trioxide) 三氧化砷(arsenic trioxide)為我國古老藥方,最近在中國被發現可以治療急性前骨髓性白血病。它不會產生傳統化學療法的副作用,只有少數人會有皮疹、頭暈、疲倦、肌肉骨骼痛及輕微的高血糖。在細胞免疫學研究上發現,用三氧化砷治療急性前骨髓性白血病,可誘導CD33抗原陽性的未成熟細胞數目成等比例下降,同時伴隨著使CD11b抗原陽性的成熟細胞數目成等比例上升,並且可一直持續到完全緩解的早期。同時依據西方墨點分析,得知三氧化砷會活化硫胱氨酸蛋白脢(caspase),導致白血細胞的凋亡。
總而言之,砷似乎能強迫癌細胞老化與自然死亡,改變其原本的進程,因此砷可能是現今緩解白血病症狀的最佳成分。但是砷的作用機轉並不十分清楚。 急性淋巴球性白血病 常用的治療藥物包括: Daunorubicin、Vincristine、Prednisolone、L-asparaginase。疾病緩解後其鞏固性治療藥物包括Methotrexate、Ara-C、VP-16等。之後會再給予口服6-MP及Methotrexate進行維持性治療。由於急性淋巴球性白血病常會侵犯中樞神經系統,所以醫師可能會併用頭部放射線治療或脊髓腔內注射化學治療。骨髓移植和周邊血幹細胞移植用於急性淋巴球性白血病也有不錯的成效。 慢性骨髓性白血病 治療開始是以 Busulfan、Hydroxuurea之類的化學藥物,即可達到緩解。部份病患在使用干擾素後有30~40%達到緩解,且存活時間也較長,但通常無法根治。高劑量化學治療合併骨髓移植是唯一可以根治的療法,成功率可達50~65%,但此治療建議40歲以下、發病時間短、預後較佳的病患可考慮。 α型干擾素治療
化學治療可使白血球數快速下降,達到所謂血液性的緩解,但對骨髓中病變的慢性骨髓性白血病細胞及其費城染色體通常沒有或只有短暫的影響。其實對抗癌症,除了以化療直接殺除癌細胞以外對於能影響癌細胞擴展的因子如它與周圍環境以及免疫細胞之間互動的研究,也漸受到重視。以干擾素為例,它可以作用於 慢性骨髓性白血病細胞及其周圍環境上,因而使得部份病患可以達到真正染色體性的緩解。加上近年來的臨床試驗也紛紛證實α型干擾素的治療可延長病患的存活期,減少轉化成急性期的比例,因此,IFN-α 已成為無法進行骨髓移植病患的最佳治療選擇。 治療後若出現染色體性的緩解,則應該繼續治療以維持這樣的緩解。直到證實染色體完全緩解 (即費城染色體陽性細胞完全消失)達3年後,即可慢慢減量並停藥,但需每 6個月追蹤一次染色體的變化。而英國MRC的經驗更指出,只要α型干擾素治療既使沒有染色體緩解也比沒有使用α型干擾素者存活期好,因此值得繼續治療。 慢性淋巴球性白血病 疾病早期如沒有特殊症狀,並不需急於治療,因為此時給予化學治療對整體存活率,並無明顯的增加。當症狀出現時,除了給予症狀治療外,可考慮給予化學治療。常用藥物包括: Cyclophosphamide、Chlorambucil、Prednisolone等藥物。其它抗癌新藥如:Fludarabine、2-deoxycoformycin、2-chlorodeoxyadenosine也有不錯的療效。 |